- Seit in den letzten Jahren die CBD-reichen Sorten eingeführt wurden, haben sich die Spielregeln des Cannabismarkts radikal verändert.
- Aufgrund seiner medizinischen Eigenschaften, aber auch seiner Vorteile für den Genussmittelkonsum hat das Cannabinoid die anderen Cannabis-Bestandteile (außer THC) mittlerweile im Bekanntheitsgrad fast überflügelt.
- Bevor wir bei Dinafem Seeds eine neue Sorte auf den Markt bringen, analysieren und selektionieren wir zuerst die jeweiligen Cannabinoid- und Terpen-Anteile unserer Genetiken. Nur so können wir garantieren, dass beide Werte unseren Ansprüchen genügen.
- Die Bedeutung von präziser Arbeit und der Forschung über die Zusammensetzung der Pflanze steht für uns außer Frage. In diesem Artikel erklären euch unsere Labortechniker, wie CBD gebildet wird.
Heutzutage weiß man, dass Cannabis, wie Leonard Fuchs im 16. Jahrhundert beschrieb, eine monotypische Gattung ist, zu der nur eine einzige Art zählt: Cannabis sativa. Dennoch ist infolge von Breeding- und Selektionsverfahren im Laufe der Jahre eine große Menge verschiedener Sorten entstanden, die sich vor allem an den Genussmittelmarkt richten. Besonderen Ruf genießen hier beispielsweise Critical + 2.0, Original Amnesia oder Skunk.
Momentan jedoch sind vor allem Zuchtprogramme auf dem Vormarsch, die auf Medizinalhanf abzielen und deshalb verschiedene Cannabinoide ins Blickfeld rücken, allem voran Cannabidiol (CBD), aber auch Cannabidivarin (CBDV) oder Cannabigerol (CBG). Die so entstandenen Sorten, ob nun als Genussmittel oder für therapeutische Zwecke gedacht, enthalten dieselben Cannabinoide, aber in jeweils unterschiedlichem Anteil, weshalb man besser von „Chemovaren" statt von „Kultivaren" sprechen und die verschiedenen Sorten nicht mehr länger nach ihrem Phänotyp, sondern nach ihrem Cannabinoidgehalt klassifizieren sollte.
Der Anteil an Cannabinoiden und Terpenoiden ist das, was eine Sorte einmalig macht. Meistens sammeln sich diese Stoffe in den Sekretionsdrüsen der glandulären Trichome, die sich hauptsächlich in den Blüten und Blättern der weiblichen Pflanzen befinden und für deren Aroma, Geschmack und Wirkung verantwortlich sind (2). Dennoch ist es möglich, auch in den Wurzeln Terpene zu finden, oder minimale Cannabinoid-Mengen in den Samen, Pollen und Wurzeln.
In den letzten Jahren haben manche Samenbanken, darunter auch Dinafem Seeds, sich auf die Entwicklung von Sorten mit einem hohen Anteil an CBD konzentriert, da dieses zunehmend in Mode kommende Cannabinoid sowohl für therapeutische Zwecke als auch für den Genussmittelkonsum große Vorteile bietet.
Wann wurde CBD entdeckt?
Cannabidiol wurde erstmals im Jahr 1940 isoliert (Adams) und 1963 identifiziert (Mechoulam and Shvo; 3). Sein chemischer Aufbau ähnelt dem von THC, weshalb in saurem Zustand eine Isomerisierung, sprich, seine Umwandlung in THC durch eine chemische Reaktion, möglich ist. Im menschlichen Körper passiert dies jedoch nicht, da der pH-Wert des Magens nicht sauer genug ist.
Bislang sind mehr als 113 Cannabinoide entdeckt und dokumentiert worden, wobei es sich jedoch bei manchen um Abbauprodukte handelt, die nur in winzigen Mengen in der Pflanze vorkommen (4). In diesem Artikel beschäftigen wir uns mit der Synthese von CBD.
Wie wird CBD gebildet?
Im Laufe der Jahre hat man neue Erkenntnisse gewonnen, dank der der Prozess der Biosynthese, der die Bildung von Cannabinoiden ermöglicht, heute besser verstanden wird. So konnte auch nachgewiesen werden, dass es einen chemischen Zusammenhang zwischen diesen Verbindungen und den Terpenoiden gibt, da beide einen gemeinsamen „Vorläufer" haben: Isopentenylpyrophosphat (IPP), das seinerseits auf Fettsäuren zurückgeht (5). Diese strukturelle Ähnlichkeit ist auch der Grund dafür, warum β-Caryophyllen (Sesquiterpenoid) an den CB2-Rezeptor bindet und auf den menschlichen Körper wirkt und warum der Verzehr von Fettsäuren das Endocannabinoidniveau im Körper verändern kann.
Die Biosynthese von CBD erfolgt in den Trichomen, härchenförmigen, aus einer Zelle bestehenden Drüsenstrukturen auf der Pflanzenepidermis, und hat viel mit der Biosynthese der Terpene gemeinsam. Deshalb wird auch davon ausgegangen, dass es eine Verbindung zwischen beiden Inhaltsstoffen gibt. Im Laufe der Biosynthese von CBD reagiert Olivetolsäure mit Geranylpyrophosphat, wobei auch das Enzym CBDA-Synthase eine wichtige Rolle spielt. Dabei bildet sich der „Vorläufer" des eigentlichen Cannabinoids, das sogenannte CBDA oder Cannabidiolsäure. Bei seiner Decarboxylierung (Abspaltung des CO2-Moleküls) schließlich entsteht CBD. Dieser Prozess wird meistens durch UV-Strahlen, Wärme oder eine zu lange Lagerung in Gang gesetzt. Das ist der Grund, warum CBDA vor allem im frischen Cannabis vorliegt und während des Trocknens oder Rauchens zu CBD umgewandelt wird.
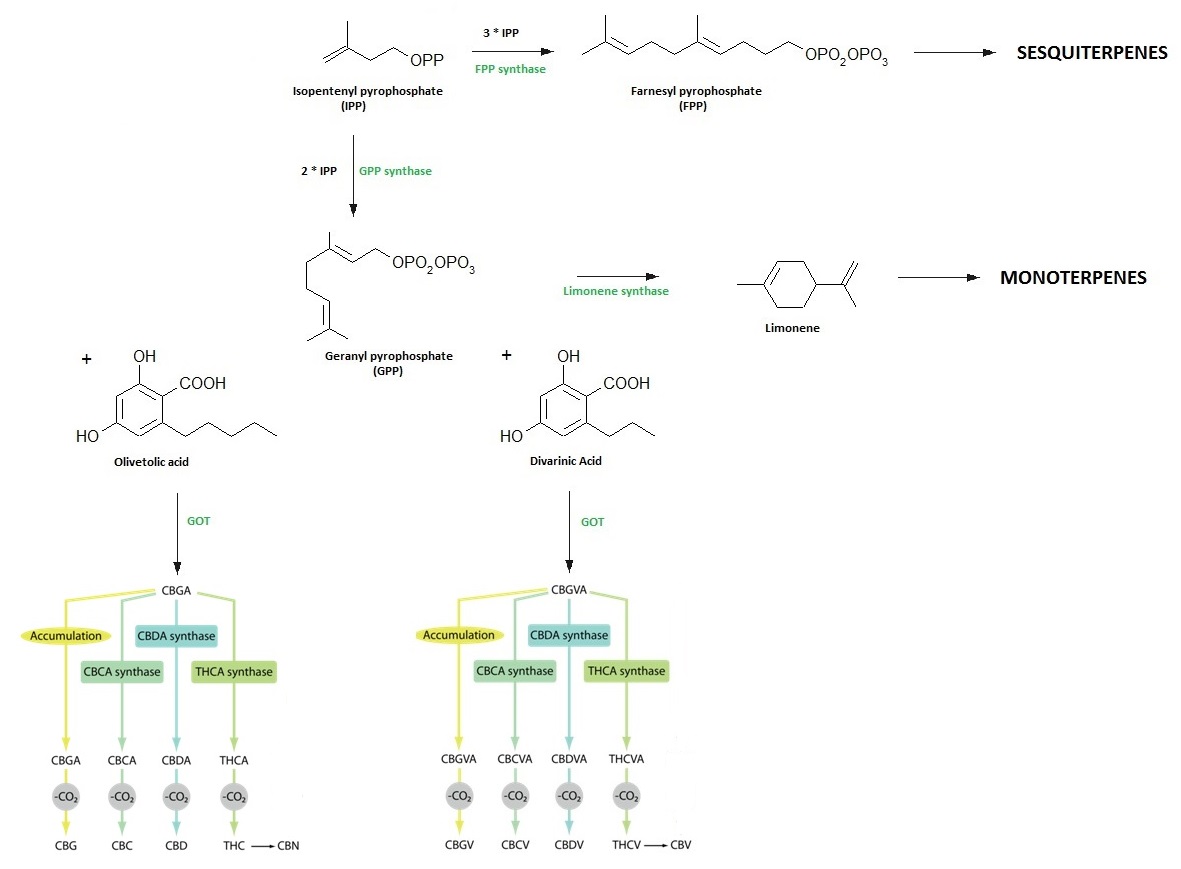
Wie bereits erwähnt, können aus der Vorstufe IPP sowohl Cannabinoide als auch Terpene entstehen. Bei der Produktion von Cannabinoiden und Monoterpenen wird IPP zunächst in Geranylpyrophosphat (GPP) umgewandelt, bei der von Sesquiterpenen hingegen in Farnesylpyrophosphat (FPP).
Diese Zwischenstoffe wiederum reagieren anschließend je nach Biosynthese-Typ mit unterschiedlichen anderen Verbindungen und Enzymen. Daraus entstehen zwei Hauptcannabinoide in saurer Form, CBGVA und CBGA, die später zu anderen sauren Cannabinoiden umgewandelt werden, wobei die Einwirkung von CBDA-Synthase zu CBDA führt, die von THCA-Synthase zu THC und die von CBCA-Synthase zu CBCA. Die Expression dieser Enzyme ist auf Gene zurückzuführen, die in verschiedenen Pflanzen in unterschiedlicher Menge vorliegen, weshalb auch die Cannabinoidanteile sich voneinander unterscheiden und jede Sorte ein einmaliges Cannabinoidprofil besitzt.
Genau hier setzen Breeding- und Selektionsverfahren an: Die Arbeit von Breedern besteht darin, Pflanzen mit bestimmten Zielmerkmalen miteinander zu kreuzen, um daraus neue Generationen zu erhalten, die ihrerseits das für besagtes Merkmal verantwortliche Gen und deshalb das erwünschte Cannabinoidprofil mitbringen. Sind die Blüten richtig getrocknet und „gecurt" worden, ohne Wärme- oder Lichtexzesse, so liegen die Cannabinoide in ihnen schließlich hauptsächlich in saurer Form vor.
Da es sich nicht um eine enzymatische Reaktion handelt, gilt die Decarboxylierung der Cannabinoide (Abspaltung der COOH-Gruppe) als Verfallsprozess. Dies kann bereits in der Pflanze selbst beginnen, geschieht gewöhnlicherweise aber, wenn die Blüten geraucht oder gebacken werden (bei der Zubereitung von Lebensmitteln). Erst dann entstehen THC, CBD, CBD und CBD, die „aktiven Formen" der Cannabinoide. Auch CBN, das durch den Abbau von THC entsteht, ist ein Verfallsprodukt und ein klares Zeichen für die Zersetzung der Pflanze (6).
Dank des wissenschaftlichen Fortschritts sind die Biosynthese-Prozesse in der Marihuana-Pflanze heutzutage nicht mehr die einzige Quelle für Cannabinoide. Mikroorganismen wie Hefezellen oder Bakterien können durch die Einschleusung der Gene, die das für die Produktion des jeweiligen gewünschten Stoffs zuständige Enzym kodieren, genetisch verändert und auf die Cannabinoidbildung programmiert werden (7). Dies ermöglicht die Synthese eines konkreten Cannabinoids oder einer Cannabinoid-Gruppe – eine hochinteressante Alternative für den therapeutischen Markt, da so standardisierte Arzneimittel von hohem Reinheitsgrad produziert werden können, was sehr viel schwieriger ist, wenn die Cannabinoide aus den Pflanzen extrahiert oder mittels chemischer Synthese erzeugt werden.
Es bleibt lediglich noch abzuwarten, ob diese Technik in großem Maßstab angewendet werden kann, sodass die Cannabinoidproduktion mittels Mikroorganismen auch wirklich rentabel ist – denn gerade an große Mengen der Verbindungen zu kommen ist die Herausforderung, die es jetzt dringend zu meistern gilt.
- Hazekamp. Chemistry of Cannabis. Comprehensive Natural Products II. (Eds: L. Mander, H-W. Lui). Elsevier, Oxford, 2010, 3, pp. 1033-1084.
- Hazekamp; J.T. Fichedick. Cannabis – from cultivar to chemovar. Drug. Test. Anal. 2012, 4, 660-667.
- G. Pertwee. Cannabinoid pharmacology: the first 66 years. Br. J. Pharmacol. 2006, 147, S163-S171.
- Aizpurua-Olaizola, et al. Evolution of the Cannabinoid and Terpene Content during the Growth of Cannabis sativa Plants from Different Chemotypes. J Nat Prod. 2016, 79, 324-331.
- Russo. Taming THC: potential cannabis synergy and phytocannabinoid-terpenoid entourage effects. Br J Pharmacol. 2011, 163, 1344–1364.
- Aizpurua-Olaizola, et al. Identification and quantification of cannabinoids in Cannabis sativa L. plants by high performance liquid chromatography-mass spectrometry. Anal Bioanal Chem. 2014, 406, 7549-7560.
- L. Poulos; A.N. Farnia. Production of cannabinoids in yeast. US20160010126A1 patent, 2017.



Kommentare unserer Leser
Noch keine Kommentare vorhanden. Wollt ihr die ersten hinterlassen?
Kommentar hinterlassenHat dieser Post dir gefallen?
Deine Erfahrungen mit unseren Samen sind sehr wichtig für uns und können anderen Usern weiterhelfen. (Deine E-Mail-Adresse wird nicht veröffentlicht.)