- Un décret modifiant l’article R.5132-86 du code de la santé publique a été signé ce 5 juin par le premier ministre français ainsi que par la ministre des affaires sociales et de la santé. Ce décret permet à l’Agence Nationale de Sécurité du Médicament (ANSM) d’étudier et de mettre sur le marché des médicaments contenant du cannabis ou ses dérivés naturels. Ce décret, conforme aux directives Européennes et est en vigueur depuis le lendemain de sa signature. A ce jour il n’y a encore aucun médicament contenant du cannabis ou ses dérivés naturels ayant reçu une autorisation de mise sur le marché (AMM). Ce décret ne modifie en rien la loi concernant la consommation ou la production de cannabis médicinal sous forme florale.En février dernier, la ministre française des affaires sociales et de la santé Marisol Touraine, s’était déclarée favorable à l’étude du Sativex® par l’ANSM.
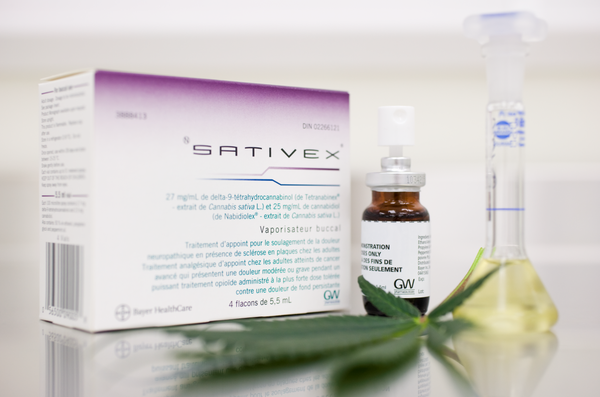
Le Sativex® est un spray buccal contenant des cannabinoides naturels, principalement du Δ-9-tétrahydrocannabinol (Δ-9-THC) ainsi que du cannabidiol (CBD). Cette préparation a été mise au point par les laboratoires « GW » et ces cannabinoides y sont présents à concentration égale (1/1). Son utilisation a été démontrée efficace dans le traitement des douleurs perçues par les patients atteints de sclérose en plaque. L'action antalgique et anti-inflammatoire produite par la synergie des deux cannabinoides combinés, s'avère réduire les contractures musculaires dues à la pathologie. Son action est également approuvée par les patients souffrant de douleurs neuropathiques.
Nous espérons que ce dernier sera rapidement commercialisé à un prix raisonnable afin d'offrir des solutions aux patients résistants aux traitements conventionnels. Ce décret permet également au monde scientifique français d'entreprendre des recherches sur l'action des cannabinoides.
Des médicaments à base de dérivés synthétiques de cannabis tel que le Dronabinol® avaient déjà reçu une autorisation temporaire ces dix dernières années. Ce médicament comme le Nabilone® contient un analogue synthétique du Δ-9-THC, permettant de réduire les nausées et vomissements des patients sous chimiothérapie.
Le nouveau décret n° 2013-473 permet donc à L'Agence de sécurité du médicament d'octroyer le droit de mise sur le marché des médicaments à base de cannabis et de ses dérivés naturels, ainsi que la fabrication, le transport, l'importation et l'exportation, la détention, l'offre et la cession ainsi que l'emploi de ces médicaments.
Bien sûr le tout, sous ordonnance.
Plus d'informations sur http://www.gwpharm.com/publications.aspx



Commentaires de nos lecteurs
Il n’y a pour l’instant aucun commentaire. Vous voulez être le premier ?
Laissez un commentaire !Vous avez aimé ce post ?
Votre expérience avec nos graines est très importante pour nous, et peut aider d'autres usagers (votre adresse e-mail ne sera pas publiée).